「禁忌を含む注意事項等情報」等は、ドラッグインフォメーションをご参照ください。
ボカブリア水懸筋注およびリカムビス®水懸筋注は、海外臨床データに基づき承認されたため、審査で評価された海外臨床試験の結果を紹介します。
ATLAS-2M試験(海外データ)
ウイルス学的抑制が得られている成人HIV-1感染症患者を対象とした非盲検比較検証試験(非劣性試験)
安全性
経口導入期(投与4週まで)における有害事象
CAB経口剤30mg+RPV経口剤25mg 1日1回経口投与による経口導入期において、Q8W群の28%(91/328例)、Q4W群の36%(118/327例)に有害事象が認められました。主な有害事象(いずれかの群における発現率≧2%)は、Q8W群で頭痛3%(10/328例)、下痢3%(9/328例)、咳2%(7/328例)、鼻咽頭炎2%(6/328例)、上気道感染症2%(5/328例)、悪心<1%(2/328例)、疲労<1%(1/328例)、Q4W群で疲労3%(11/327例)、頭痛2%(7/327例)、鼻咽頭炎2%(6/327例)、上気道感染症2%(6/327例)、悪心2%(6/327例)、下痢2%(5/327例)、咳<1%(3/327例)でした。
なお、重篤な有害事象は、Q8W群で1例1件(椎間板突出1件)、Q4W群で4例4件(肺炎、唾液腺炎、副鼻腔炎の再発、自然流産各1件)に認められましたが、いずれも治験薬との因果関係は否定されました。投与中止に至った有害事象は、Q8W群で2例2件(無力症、皮膚病変各1件)、Q4W群で2例3件(疲労、トランスアミナーゼ上昇、うつ各1件)に認められ、無力症、疲労及びうつ、並びにトランスアミナーゼ上昇が治験薬と因果関係ありと判断されました。経口導入期において死亡は認められませんでした。
Q8W:8週間隔投与、Q4W:4週間隔投与
維持療法期における副作用、重篤な副作用、投与中止に至った有害事象、死亡
投与48週後の副作用発現率は、Q8W群で77%(400/522例)、Q4W群で76%(399/523例)であり、注射部位反応を除くとQ8W群で21%(109/522例)、Q4W群で24%(125/523例)でした。注射部位反応を除く主な副作用(いずれかの群における発現率≧1%)は表の通りでした。
なお、重篤な副作用は、Q8W群で3例3件(注射部位膿瘍、失神寸前の状態、急性膵炎各1件)、Q4W群で1例1件(過敏症1件)に認められました。投与中止に至った有害事象は、Q8W群で12例18件(注射部位疼痛、疲労、注射部位腫脹、発熱、無力症、注射部位変色、注射部位不快感、注射部位過敏症、注射部位壊死、注射部位熱感、頭痛、失神寸前の状態、急性B型肝炎、注射部位膿瘍、斑丘疹発疹、皮膚病変、急性膵炎、びまん性大細胞型B細胞リンパ腫各1件)、Q4W群で13例28件(注射部位疼痛4件、疲労、多汗症、異常な夢各2件、注射部位腫脹、発熱、悪寒、注射部位結節、頭痛、失神寸前の状態、注意障害、浮動性めまい、急性B型肝炎、インフルエンザ、抑うつ、不眠、睡眠障害、悪心、神経膠芽腫、過敏症、トランスアミナーゼ上昇、筋肉痛各1件)に認められました。死亡は、維持療法期においてQ8W群の1例に認められ、急性膵炎後の敗血症でしたが、治験薬との因果関係は否定されました。また、スクリーニング期に1例の死亡が認められましたが、治験薬は投与されておらず、脳動脈瘤からの出血が原因でした。
投与96週後の副作用発現率は、Q8W群で80%(415/522例)、Q4W群で79%(413/523例)であり、注射部位反応を除くとQ8W群で23%(122/522例)、Q4W群で28%(146/523例)でした。注射部位反応を除く主な副作用(いずれかの群における発現率≧1%)は表の通りでした。
なお、重篤な副作用は、Q8W群で4例4件(急性膵炎、注射部位腫瘍、骨壊死、失神寸前の状態各1件)、Q4W群で3例3件(薬物過敏症、過敏症、心筋梗塞各1件)に認められました。投与中止に至った有害事象は、Q8W群で18例24件(注射部位疼痛、頭痛各2件、疲労、注射部位腫脹、発熱、無力症、注射部位変色、注射部位不快感、注射部位壊死、注射部位熱感、倦怠感、失神寸前の状態、多汗症、斑丘疹発疹、皮膚病変、急性膵炎、急性B型肝炎、注射部位膿瘍、乳癌、びまん性大細胞型B細胞リンパ腫、精巣腫瘍、骨壊死各1件)、Q4W群で20例37件(注射部位疼痛4件、疲労、注意障害、異常な夢、睡眠障害、多汗症、悪心、筋肉痛各2件、注射部位腫脹、発熱、悪寒、注射部位結節、頭痛、失神寸前の状態、浮動性めまい、自殺、抑うつ、不眠、痔核、急性B型肝炎、インフルエンザ、神経膠芽腫、薬物過敏症、過敏症、心筋梗塞、回転性めまい、トランスアミナーゼ上昇各1件)に認められました。死亡は、Q8W群で1例(敗血症)、Q4W群で1例(自殺)に認められましたが、治験薬との因果関係は否定されました。
投与152週後の副作用発現率は、Q8W群で82%(427/522例)、Q4W群で82%(427/523例)であり、注射部位反応を除くとQ8W群で27%(142/522例)、Q4W群で32%(167/523例)でした。注射部位反応を除く主な副作用(いずれかの群における発現率≧1%)は表の通りでした。
なお、96週目以降、重篤な副作用は報告されませんでした。投与中止に至った有害事象は、Q8W群で23例(4%)、Q4W群で25例(5%)で、そのうち96週目以降ではQ8W群で5例(1%)、Q4W群で6例(1%)でした。96週目以降の死亡は、 Q8W群で2例(自殺、膵臓がん)、Q4W群で2例(心停止、慢性閉塞性肺疾患/慢性腎不全)に認められましたが、治験薬との因果関係は否定されました。
●注射部位反応を除く主な副作用の発現率(投与48週後、96週後および152週後、安全性解析対象集団)(いずれかの群における発現率≧1%)
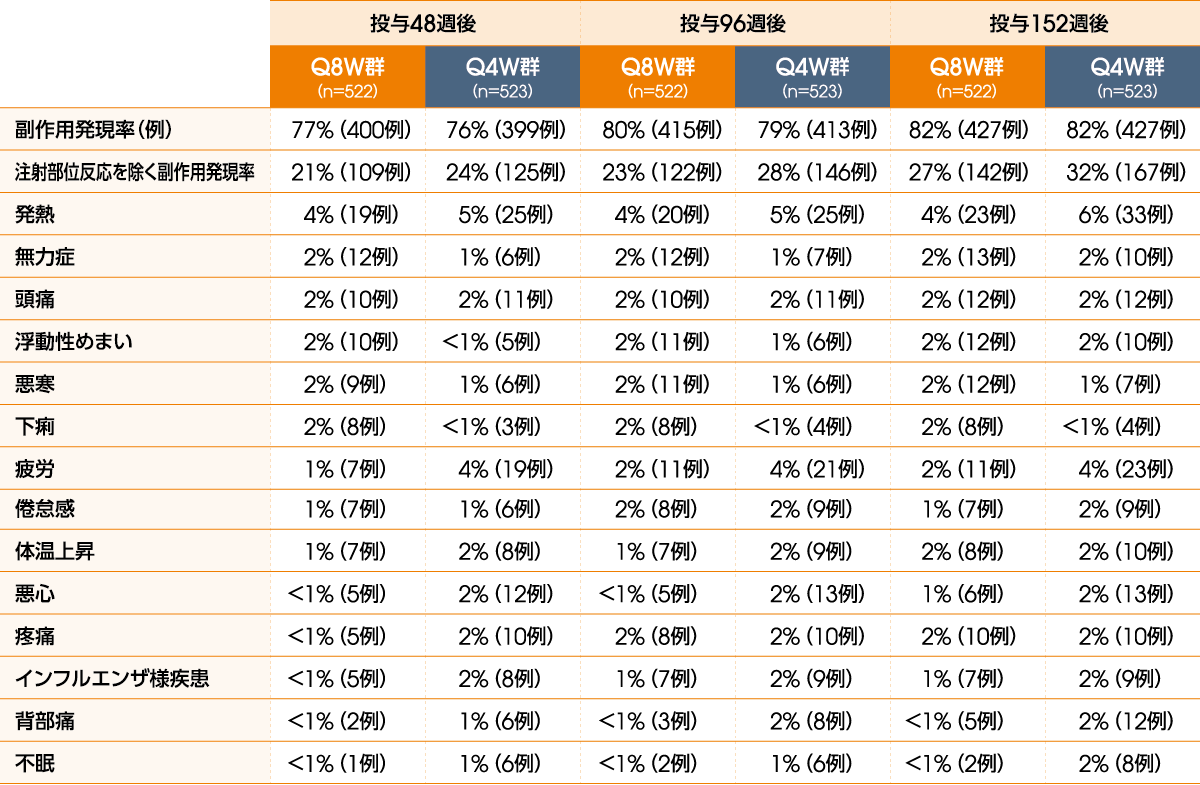
Q8W:8週間隔投与、Q4W:4週間隔投与
注射部位反応
●注射部位反応の発現数(投与48週後、96週後および152週後、安全性解析対象集団)
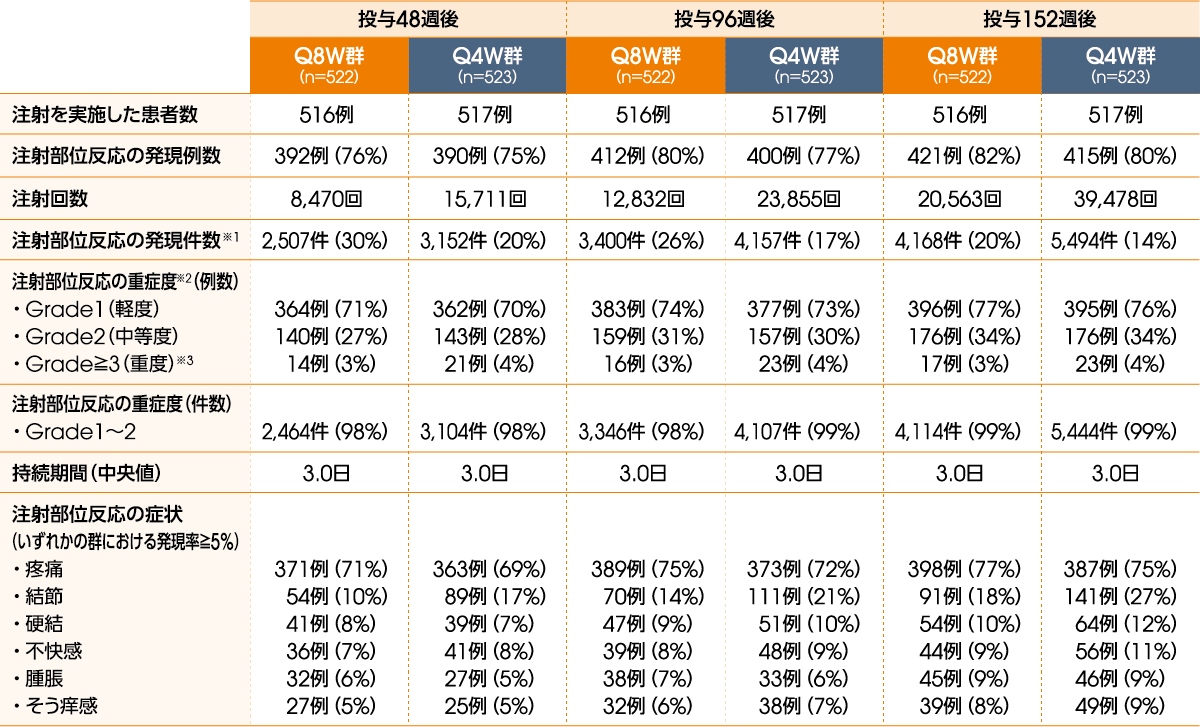
Q8W:8週間隔投与、Q4W:4週間隔投与
※1 注射部位反応の発現件数の割合は、注射回数から算出した。1回の注射で1件以上の注射部位反応が認められた。
※2 Grade1:症状を伴う/伴わない圧痛(例:熱感、紅斑、そう痒)、Grade2:疼痛;脂肪変性;浮腫;静脈炎、Grade3:潰瘍または壊死;高度の組織損傷;外科的処置を要する、Grade4:生命を脅かす;緊急処置を要する、Grade5:死亡 [有害事象共通用語規準 v5.0日本語訳JCOG版]
※3 Grade4~5の注射部位反応は認められなかった。
●注射部位反応の発現率(投与152週まで、安全性解析対象集団)
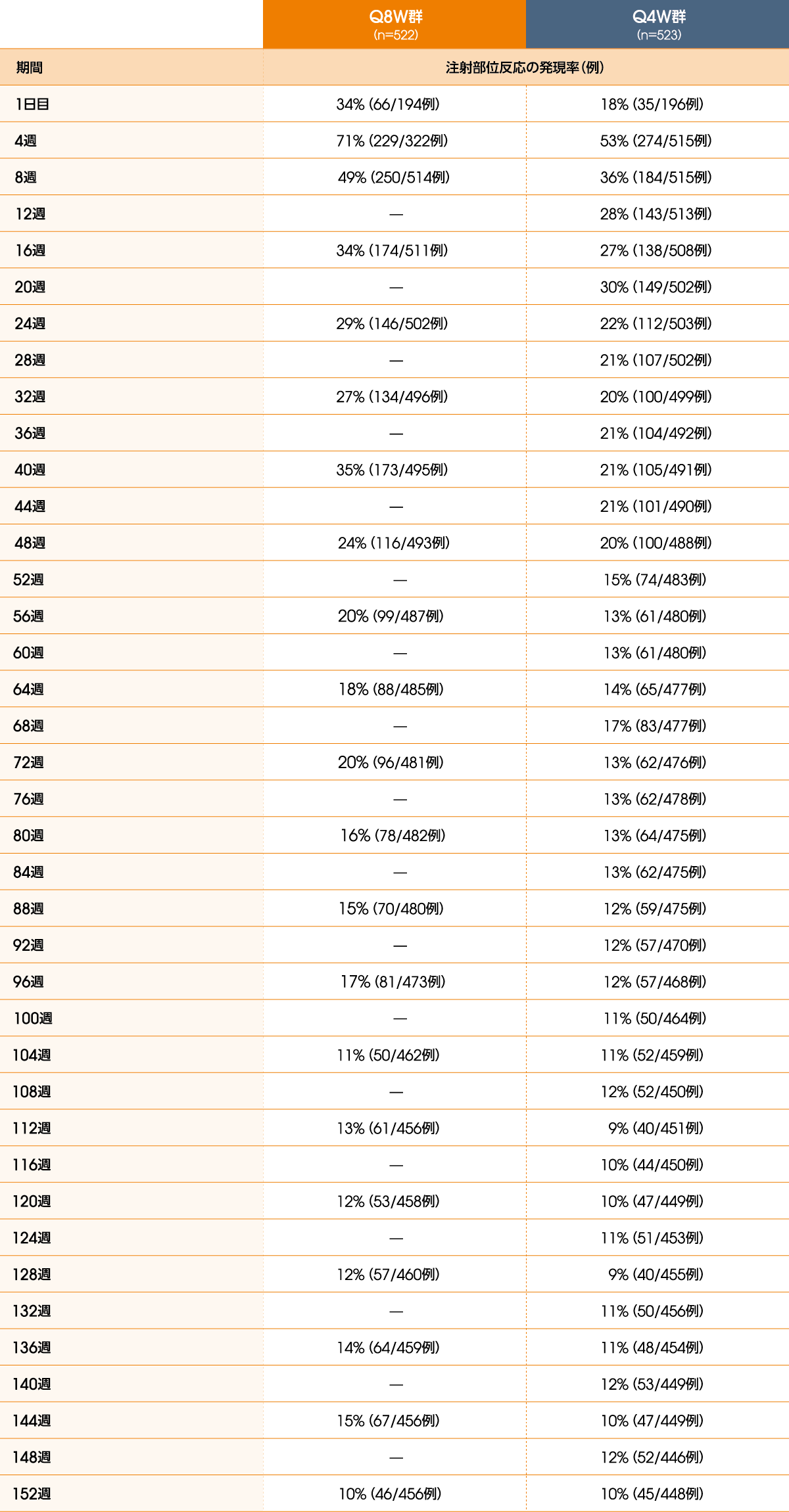
Q8W:8週間隔投与、Q4W:4週間隔投与
本邦で承認されたボカブリア水懸筋注およびリカムビス®水懸筋注の用法及び用量は、 1ヵ月間隔投与(CAB注射剤600mg及びRPV注射剤900mgを投与し、以降はそれぞれ400mg、600mgを1ヵ月に1回投与)および2ヵ月間隔投与(CAB注射剤600mg及びRPV注射剤900mgを投与し、初回投与後1ヵ月後にそれぞれ600mg、900mgを投与、以降はそれぞれ600mg、900mgを2ヵ月に1回投与)です。
引用文献
- Overton, E.T., et al.: Lancet 396(10267), 1994-2005(2020)
[本試験に関する費用は、ヴィーブヘルスケア(株)及びヤンセンファーマ(株)の支援を受けた。著者には、ヴィーブヘルスケア(株)及びヤンセンファーマ(株)の社員が含まれる。] - Jaeger, H., et al.: Lancet HIV 8(11), e679-e689(2021)
[本試験に関する費用は、ヴィーブヘルスケア(株)及びヤンセンファーマ(株)の支援を受けた。著者には、ヴィーブヘルスケア(株)及びヤンセンファーマ(株)の社員が含まれる。] - Overton,E.T.,et al.:Clin Infect Dis 76(9),1646-1654(2023)
[本試験に関する費用は、ヴィーブヘルスケア(株)及びヤンセンファーマ(株)の支援を受けた。著者には、ヴィーブヘルスケア(株)及びヤンセンファーマ(株)の社員が含まれる。] - 承認時評価資料:海外臨床試験(207966)
PM-JP-CBR-WCNT-220004 | 改訂年月2025年11月


