「禁忌を含む注意事項等情報」等は、ドラッグインフォメーションをご参照ください。
ボカブリア水懸筋注およびリカムビス®水懸筋注は、海外臨床データに基づき承認されたため、審査で評価された海外臨床試験の結果を紹介します。
ATLAS試験(海外データ)
ウイルス学的抑制が得られている成人HIV-1感染症患者を対象とした非盲検比較検証試験(非劣性試験)
安全性
経口導入期(投与4週まで)における有害事象
CAB経口剤30mg+RPV経口剤25mg 1日1回経口投与による経口導入期において、30%(92/308例)に有害事象の発現が認められました。主な有害事象は、鼻咽頭炎4%(12/308例)、頭痛3%(9/308例)、尿路感染症2%(6/308例)、上気道感染症2%(5/308例)、悪心2%(5/308例)、不眠症2%(5/308例)でした。頭痛は、治験薬との関連が認められました。
なお、重篤な有害事象は1例に認められ、妊娠(中絶なし)でした。投与中止に至った有害事象は、5例に認められました〔治験薬と関連のある頭痛1例、うつ病による自殺1例、プロトコールの逸脱(アドヒアランス不良2例)、妊娠1例〕。経口導入期において死亡は認められませんでした。
維持療法期における副作用、重篤な有害事象、投与中止に至った有害事象、死亡
投与52週後の副作用発現率は、CAB+RPV群で83%(255/308例)、CAR群で3%(8/308例)であり、CAB+RPV群では、注射部位反応を除くと29%(88/308例)でした。注射部位反応を除く主な副作用(いずれかの群における発現率≧3%)は、表の通りでした。
なお、重篤な有害事象は、CAB+RPV群で13例15件(A型肝炎、急性B型肝炎、大腸菌胃腸炎、肝膿瘍、急性腎盂腎炎、ウイルス感染症、急性膵炎、嘔吐、乳頭様甲状腺癌、急性胆嚢炎、肝細胞障害、高ビリルビン血症、不全流産、肝機能検査異常、背部痛各1件)、CAR群で14例17件(大腸炎2件、A型肝炎、肛門膿瘍、虫垂炎、肺炎、動物咬創、眼外傷、過量投与、頭蓋骨折、肛門性器疣贅、精上皮腫、自然流産、胸部不快感、脳血管発作、自殺念慮、呼吸困難各1件)に認められました。投与中止に至った有害事象は、CAB+RPV群で13例18件(注射部位疼痛4件、A型肝炎、頭痛各2件、無力症、注射部位結節、注射部位腫脹、急性B型肝炎、記憶障害、不安、うつ病による自殺、下痢、悪心、筋肉痛各1件)、CAR群で5例7件(不安障害、抑うつ、自殺念慮、大腸炎、血中クレアチニン増加、過量投与、腎機能障害各1件)に認められました。死亡は、CAR群の1例に認められましたが、メタンフェタミンの過量投与であり、治験薬との因果関係は否定されました。
●注射部位反応を除く主な副作用の発現率(投与52週後、安全性解析対象集団)(いずれかの群における発現率≧3%)

注射部位反応
投与52週後における注射部位反応は、CAB+RPV群で83%(250/303例)に認められました。主な注射部位反応(副作用)は、注射部位疼痛74%(227/303例)でした。症状の持続期間は、3.0日(中央値)でした。
CAB+RPV群における投与48週までの注射部位反応の発現率は表の通りでした。
●注射部位反応の発現数(投与52週後、安全性解析対象集団)
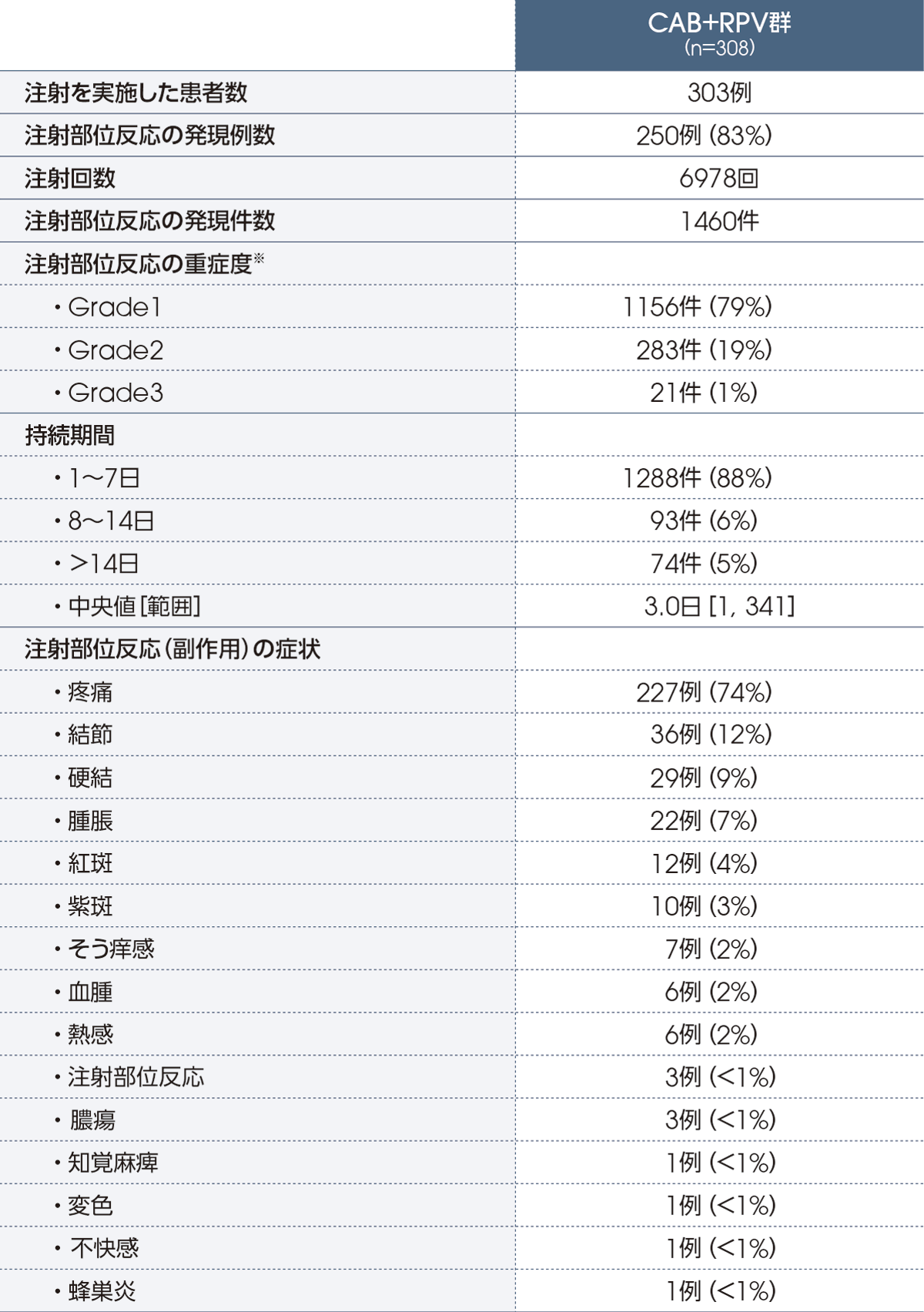
※ Grade1:症状を伴う/伴わない圧痛(例:熱感、紅斑、そう痒)、Grade2:疼痛;脂肪変性;浮腫;静脈炎、Grade3:潰瘍または壊死;高度の組織損傷;外科的処置を要する、Grade4:生命を脅かす;緊急処置を要する、Grade5:死亡[有害事象共通用語規準 v5.0日本語訳JCOG版]
●CAB+RPV群における注射部位反応の発現率(投与48週まで、安全性解析対象集団)

本邦で承認されたボカブリア水懸筋注およびリカムビス®水懸筋注の用法及び用量は、 1ヵ月間隔投与(CAB注射剤600mg及びRPV注射剤900mgを投与し、以降はそれぞれ400mg、600mgを1ヵ月に1回投与)および2ヵ月間隔投与(CAB注射剤600mg及びRPV注射剤900mgを投与し、初回投与後1ヵ月後にそれぞれ600mg、900mgを投与、以降はそれぞれ600mg、900mgを2ヵ月に1回投与)です。
引用文献
- Swindells, S., et al.:N Engl J Med 382(12), 1112-1123(2020)
[本試験に関する費用は、ヴィーブヘルスケア(株)及びヤンセンファーマ(株)の支援を受けた。著者には、ヴィーブヘルスケア(株)及びヤンセンファーマ(株)の社員が含まれる。] - 承認時評価資料:海外臨床試験(201585)
PM-JP-CBR-WCNT-220004 | 改訂年月2025年11月


