「禁忌を含む注意事項等情報」等は、ドラッグインフォメーションをご参照ください。
ボカブリア水懸筋注およびリカムビス®水懸筋注は、海外臨床データに基づき承認されたため、審査で評価された海外臨床試験の結果を紹介します。
LATTE-2試験(海外データ)
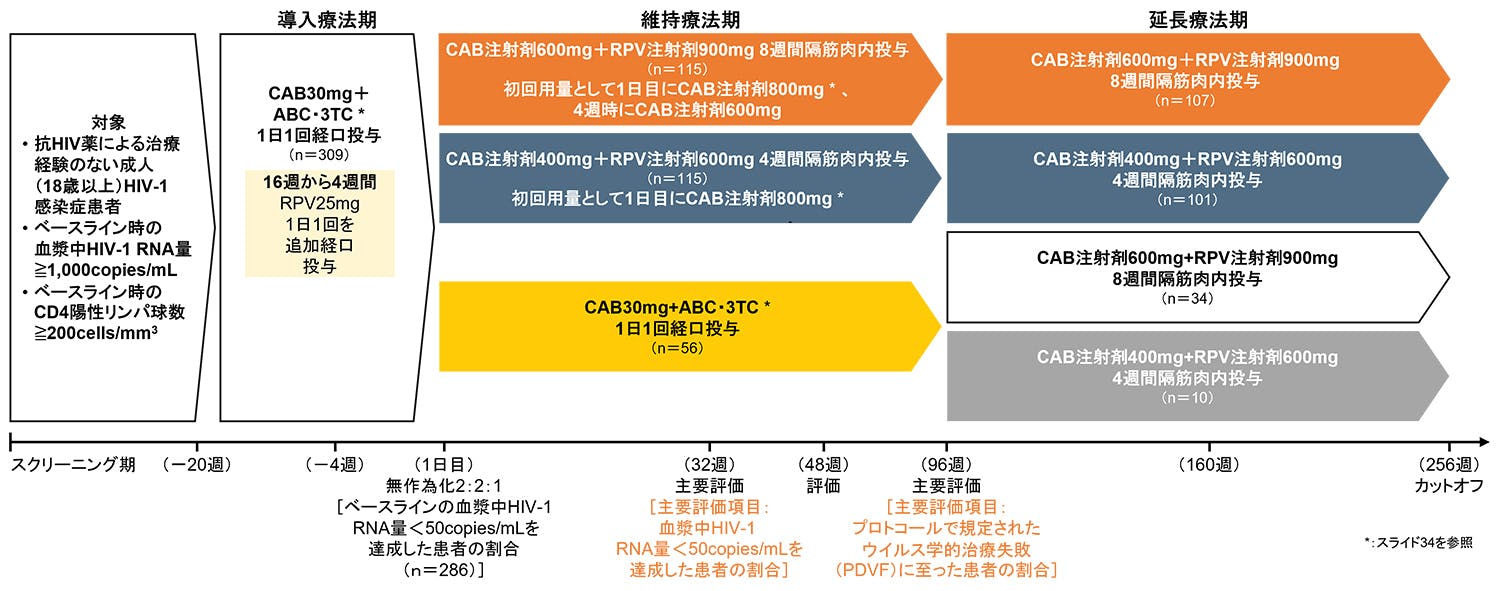
抗HIV薬による治療経験のない成人HIV-1感染症患者を対象とした用量設定試験(非劣性試験)
試験デザイン
多施設共同、無作為化、非盲検、並行群間比較、第Ⅱb相用量設定試験(非劣性試験)(カナダ、フランス、ドイツ、スペイン、米国の50ヵ所で実施)
患者背景(ITT-ME集団)
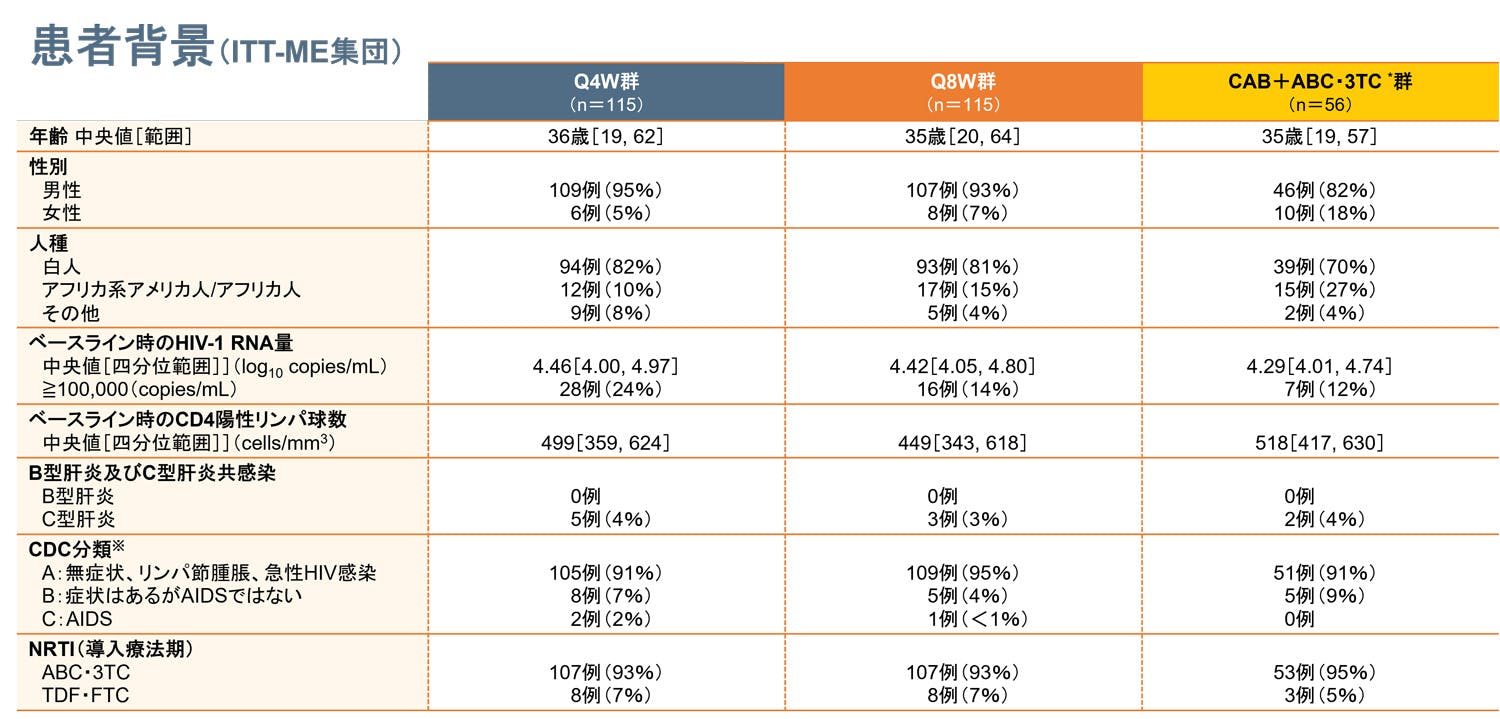
Q4W:4週間隔投与、Q8W:8週間隔投与、NRTI:核酸系逆転写酵素阻害剤、ABC:アバカビル、3TC:ラミブジン、TDF:テノホビル、FTC:エムトリシタビン
※ Stage1:HIV感染検査陽性でAIDSと定義される状態ではなくCD4陽性Tリンパ球数≧500cells/μLまたはCD4陽性Tリンパ球数が全リンパ球数の≧26%の場合
Stage2:HIV感染検査陽性でAIDSと定義される状態ではなくCD4陽性Tリンパ球数200~499cells/μLまたはCD4陽性Tリンパ球数が全リンパ球数の14%~25%の場合
Stage3:HIV感染検査陽性でCD4陽性Tリンパ球数が<200cells/μLまたはCD4陽性Tリンパ球数が全リンパ球数の<14%またはAIDSと定義される状態の場合
本邦で承認されたボカブリア水懸筋注およびリカムビス®水懸筋注の用法及び用量は、1ヵ月間隔投与(CAB注射剤600mg及びRPV注射剤900mgを投与し、以降はそれぞれ400mg、600mgを1ヵ月に1回投与)および2ヵ月間隔投与(CAB注射剤600mg及びRPV注射剤900mgを投与し、初回投与後1ヵ月後にそれぞれ600mg、900mgを投与、以降はそれぞれ600mg、900mgを2ヵ月に1回投与)です。
引用文献
- Margolis, D.A., et al.: Lancet 390(10101), 1499-1510(2017)
[本試験に関する費用は、ヴィーブヘルスケア(株)及びヤンセンファーマ(株)の支援を受けた。著者には、ヴィーブヘルスケア(株)及びヤンセンファーマ(株)による助成金等を受けた者が含まれる。著者には、ヴィーブヘルスケア(株)及びヤンセンファーマ(株)の社員が含まれる。] - 承認時評価資料:海外臨床試験(200056)
PM-JP-CBR-WCNT-220004 | 改訂年月2025年11月


