「禁忌を含む注意事項等情報」等は、ドラッグインフォメーションをご参照ください。
ボカブリア水懸筋注およびリカムビス®水懸筋注は、海外臨床データに基づき承認されたため、審査で評価された海外臨床試験の結果を紹介します。
LATTE-2試験(海外データ)
抗HIV薬による治療経験のない成人HIV-1感染症患者を対象とした用量設定試験(非劣性試験)
有効性
抗ウイルス効果(ITT-ME集団)
投与32週後に血漿中HIV-1 RNA量<50copies/mLを達成した患者の割合は、ITT-ME集団において、Q4W群で94%(108/115例)、Q8W群で95%(109/115例)、CAB+ABC・3TC *群で91%(51/56例)でした(FDA Snapshotアルゴリズム解析)。Q4W群及びQ8W群は、CAB+ABC・3TC *経口投与群に対する非劣性を検討するための事前に規定された有効性の基準を満たしていました(事後確率>90%;ベイズ解析)。投与32週後におけるCAB+ABC・3TC *群との差は、Q4W群で2.8%[95%信頼区間:-5.8%, 11.5%]、Q8W群で3.7%[95%信頼区間:-4.8%, 12.2%]でした。
● 血漿中HIV-1 RNA量<50copies/mLを達成した患者の割合(投与32週後、96週後および256週後、ITT-ME集団)
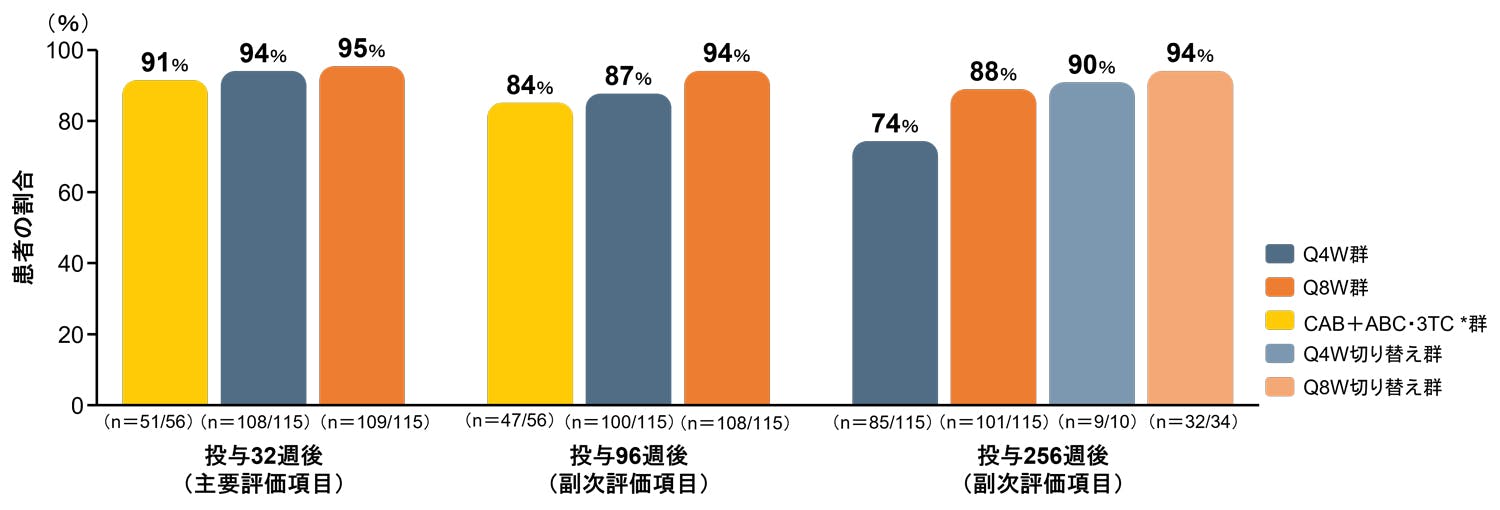
Q4W:4週間隔投与、Q8W:8週間隔投与
投与256週後に血漿中HIV-1 RNA量<50copies/mLを達成した患者の割合は、ITT-ME集団において、Q4W継続群で74%(85/115例)、Q8W継続群で88%(101/115例)でした(FDA Snapshotアルゴリズム解析)。
● 血漿中HIV-1 RNA量<50copies/mLを達成した患者の割合(投与32週後、ITT-ME集団)【主要評価項目】
● 血漿中HIV-1 RNA量<50copies/mLを達成した患者の割合(投与256週後、ITT-ME集団)【副次評価項目】
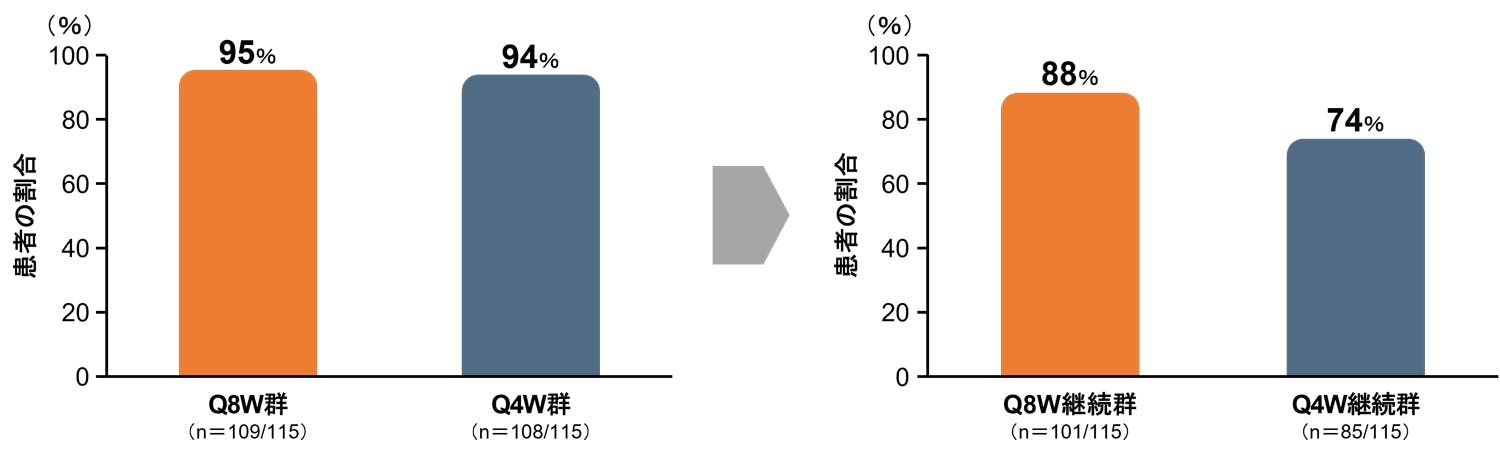
投与256週後におけるQ8W群の患者において、投与中止に至った患者は14例(12%)でした。
- 有害事象2例(2%)
- 効果不十分1例(<1%)
- その他の理由11例(10%)
Q4W:4週間隔投与、Q8W:8週間隔投与
投与256週までにPDVFが認められた患者
● プロトコールで規定されたウイルス学的治療失敗(PDVF)※に至った患者の割合(ITT-ME集団)【主要評価項目】
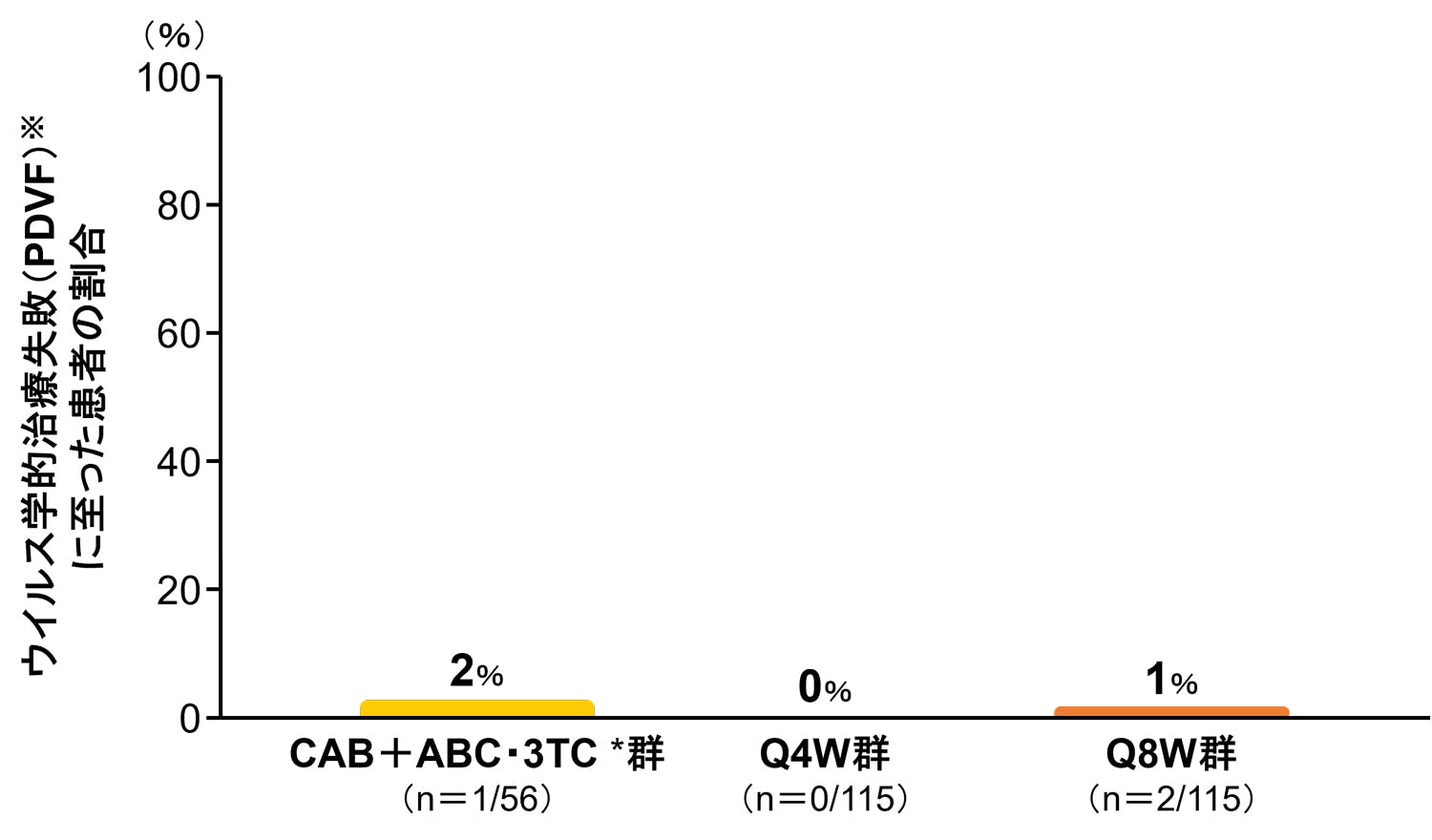
Q4W:4週間隔投与、Q8W:8週間隔投与
※ PDVF(Protocol-defined virological failure): プロトコールで規定されたウイルス学的治療失敗 定義:無作為化後、血漿中HIV-1 RNA量≧200copies/mLが2回連続して検出された場合
<参考情報>投与スケジュールの遵守率(投与256週後)
LATTE-2試験のCAB注射剤+RPV注射剤(Q8W)継続群において、ベースラインから投与256週までのすべての患者の来院数のうち96%(n=3,401/3,525)が投与スケジュール※1を遵守しました※2。
● 投与スケジュールを遵守した患者の割合(投与256週後)【副次評価項目】
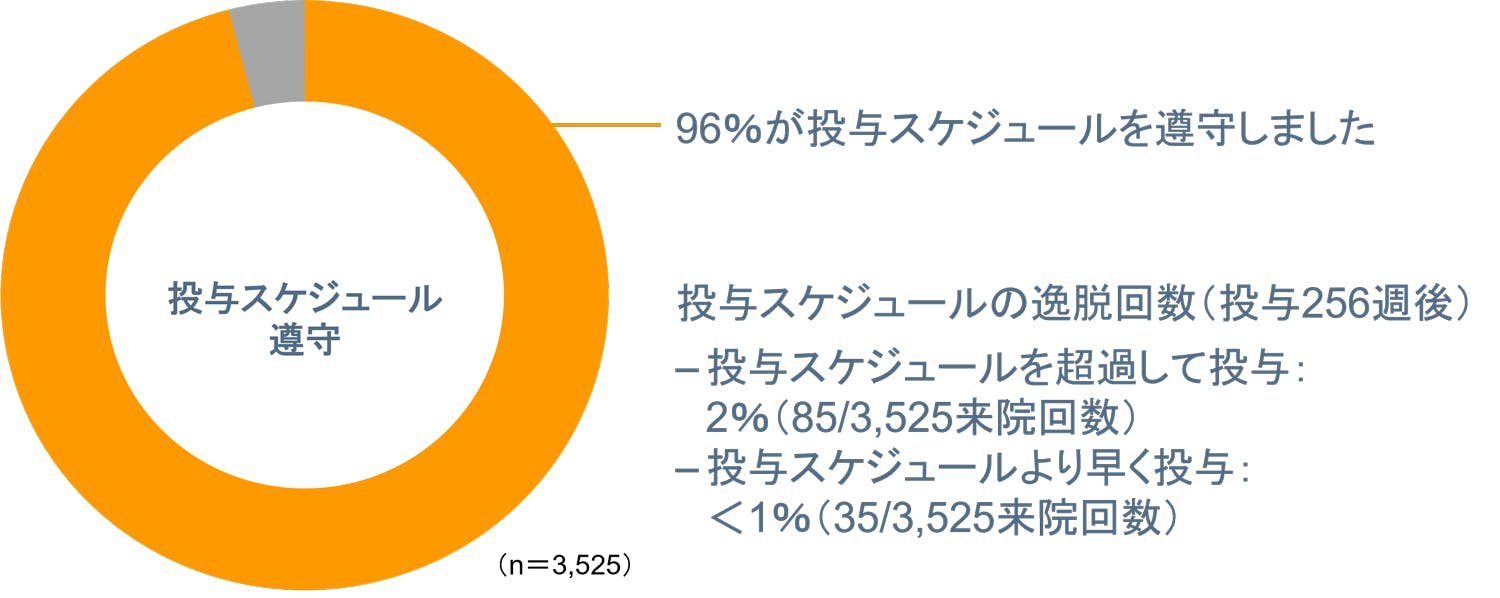
Q8W:8週間隔投与
※ 1 投与予定日から±7日
※ 2 投与スケジュールの遵守できなかった<1%(n=35/3,525)は早期、2%(n=85/3,525)は後期に認められた。そのうち経口ブリッジングを活用した2例は、256週後まで血漿中HIV-1 RNA量<50copies/mLを維持した。
本邦で承認されたボカブリア水懸筋注およびリカムビス®水懸筋注の用法及び用量は、1ヵ月間隔投与(CAB注射剤600mg及びRPV注射剤900mgを投与し、以降はそれぞれ400mg、600mgを1ヵ月に1回投与)および2ヵ月間隔投与(CAB注射剤600mg及びRPV注射剤900mgを投与し、初回投与後1ヵ月後にそれぞれ600mg、900mgを投与、以降はそれぞれ600mg、900mgを2ヵ月に1回投与)です。
引用文献
- Margolis, D.A., et al.: Lancet 390(10101), 1499-1510(2017)
- Smith, G.H.R., et al.: Open Forum Infect Dis 8(9):ofab439(2021)
[本試験に関する費用は、ヴィーブヘルスケア(株)及びヤンセンファーマ(株)の支援を受けた。 著者には、ヴィーブヘルスケア(株)及びヤンセンファーマ(株)による助成金等を受けた者が含まれる。著者には、ヴィーブヘルスケア(株)及びヤンセンファーマ(株)の社員が含まれる。] - 承認時評価資料:海外臨床試験(200056)
PM-JP-CBR-WCNT-220004 | 改訂年月2025年11月


